HIDRÓGENO COMO VECTOR ENERGÉTICO
Dado que los sistemas de almacenamiento de hidrógeno no son fuentes de energía si no vectores energéticos, siempre existen pérdidas en cada etapa del proceso de producción y almacenamiento que originan que la energía útil a la salida sea inferior a la energía de entrada al sistema. Estas pérdidas dependen fundamentalmente del tipo de sistema generador de electrólisis y su composición, más el tiempo en el que el hidrógeno permanece almacenado escapando progresivamente y reaccionando con el almacenamiento destruyendo su composición cristalina. Frecuentemente se requieren otros consumos de energía para compensar las carencias de algunos sistemas (como todos los Stacks o apilamientos sin excepción) para mantener ciertas condiciones de operación requeridas, como mantener una temperatura suficientemente baja, crear y mantener presiones, etc… Estos consumos de energía se conocen como pérdidas parásitas, por norma general todos los fabricantes omiten deliberadamente estos consumos cuando les solicitamos información sobre eficiencias y más cuando estas afectan al balance global de planta.
Las siguientes características generales son clave para las comparaciones entre los diferentes sistemas actuales:
|
-Energía por unidad de masa y de volumen. -Potencia por unidad de masa y de volumen. -Rendimiento por ciclo de carga y descarga. -Número máximo de ciclos de carga y descarga. -Vida útil y mantenimiento del sistema. |
-Tiempo de respuesta. -Rango de potencia óptimo. -Requisitos de ubicación. -Consumo de agua. -Impacto medioambiental. |
Antes de abordar la generación y el almacenamiento del hidrógeno, debemos conocer sus propiedades físicas:
– Volumen específico del hidrógeno gaseoso es 11,9 m3 /kg a 20 ºC y 1 atm.
– Volumen específico del hidrógeno líquido 0,014 m3 /kg a −253 ºC y 1 atm.
– El peso específico del hidrógeno gaseoso es 0,0696 su densidad es de tan sólo un 6,96 % la densidad del aire.
– La referencia para líquidos es el agua (1 Ton/m3 ) a 4 ºC y 1 bar, el hidrógeno líquido un 7,08 % la densidad del agua.
– La temperatura de ebullición del hidrógeno es de −240 ºC con una presión de aproximadamente 13 bar, que se corresponde con su punto crítico.
Cada metro cúbico de agua contiene 111 litros de hidrógeno. Cada metro cúbico de hidrógeno líquido contiene solo 71 kgrs de hidrógeno.
DATOS A TENER EN CUENTA PARA EL ALMACENAMIENTO
Cuando el hidrógeno se almacena en estado gaseoso a 250 bar y temperatura atmosférica 30ºC, su relación de expansión es 1:240. Por eso el almacenamiento a presión le confiere una reducción de espacio significativa pero, por encima de 800 bar, un aumento de presión apenas afecta al volumen del hidrógeno.
Las moléculas de hidrógeno gaseoso son más pequeñas que las de todos los demás gases y pueden difundirse a través de muchos materiales considerados herméticos o impermeables a otros gases. Las fugas de hidrógeno son peligrosas porque suponen un riesgo de incendio cuando se mezclan con el aire. El pequeño tamaño de la molécula de hidrógeno, le confiere una flotabilidad y difusividad muy altas, por lo que el hidrógeno filtrado se eleva y se diluye rápidamente al aire libre.
Las fugas de hidrógeno suponen un elevado riesgo de incendio cuando se mezclan con el aire. No obstante, las llamas resultantes de la combustión del hidrógeno son más seguras que las de la gasolina, debido a que el hidrógeno se eleva rápidamente debido a su mayor volatilidad y difusividad. Como consecuencia, las llamas de hidrógeno son muy localizadas y verticales. En cambio, el hidrógeno se quema más enérgicamente que la gasolina y durante un tiempo más corto.
El hidrógeno tiene una alta velocidad de llama en proporciones estequiométricas con el oxígeno, siendo la velocidad de la llama de hidrógeno un orden de magnitud más rápida que la de la gasolina. Sin embargo, en concentraciones más bajas, la velocidad de la llama disminuye significativamente pareciéndose más a la combustión de propano. Al contrario que el resto de los combustibles, el hidrógeno únicamente emite vapor de agua cuando se quema, esto le confiere el titulo del combustible más limpio que conoce el ser humano.
El hidrógeno puro es inodoro, incoloro e insípido, por lo que una fuga es prácticamente imperceptible y su detección precisa sensores específicos. El hidrógeno no es tóxico ni contaminante, pero debido a su elevada reactividad, su manipulación requiere precauciones especiales para evitar accidentes.
El hidrógeno puede actuar como asfixiante en espacios cerrados como los edificios, desplaza el volumen que ocupa el oxígeno del aire y mata rápidamente sin que el operador tenga tiempo de reacción. Es necesario evitar las edificaciones donde pueda quedar confinado el hidrógeno o extremar las medidas de seguridad y garantizar la ventilación de los espacios en los que se almacene o manipule hidrógeno.
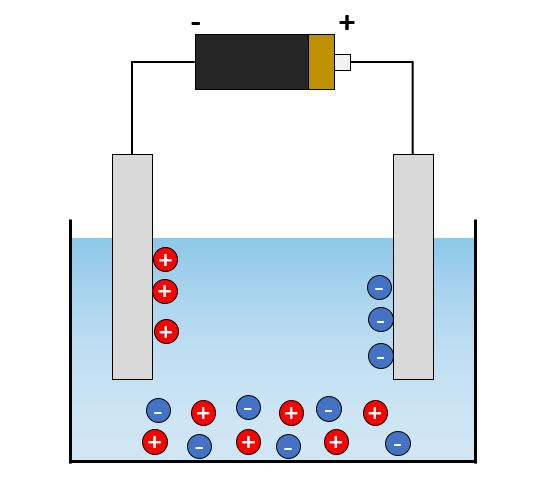
FUNDAMENTO DE UNA CELDA ELECTROLÍTICA
Las celdas de un electrolizador se asemejan a los condensadores eléctricos. Están formados por placas sumergidas en un electrolito, este conjunto almacena la energía en forma de carga eléctrica entre dos placas metálicas separadas por cierta distancia y cuando se aplica energía para superar el almacenamiento de cargas, es cuando comienza el proceso de electrólisis.
Los factores que determinan la capacitancia de las celdas son el tamaño de las placas utilizadas como electrodo, la densidad del metal que compone dichas placas, la separación entre ellas y la cantidad de electrolito contenido dentro de la celda.
La capacitancia en las celdas electrolíticas, se puede aumentar modificando ciertos aspectos de la misma. Entendemos que esta característica de capacidad está directamente relacionada con la flexibilidad ante un posible aumento espontaneo de las cargas aplicadas en las celdas. Esto se traduce en la capacidad de trabajar en un rango de voltaje mayor dejando más margen de operación y gestión de carga. Las celdas son dispositivos modulares que se pueden disponer en serie o en paralelo para aumentar la potencia y la capacidad, respectivamente.
FUNDAMENTOS DE LA ELECTRÓLISIS
La electrólisis consiste en la descomposición de una sustancia en disolución mediante el paso de una corriente eléctrica. En el caso del agua, se separa en hidrógeno y oxígeno.
Los equipos en los que se produce este proceso se denominan electrolizadores y están formados principalmente por una celda provista de un electrodo negativo o cátodo y un electrodo positivo o ánodo.
Los electrodos están sumergidos en una disolución acuosa conductora denominada electrolito. El electrolito permite el movimiento de iones de la disolución desde un electrodo hacia otro, pero impide el paso de electrones por medio de un conjunto separador. Los electrodos se polarizan utilizando corriente continua, por lo que los iones disueltos en el electrolito se dirigen hacia el electrodo de carga opuesta, donde experimentan una reacción electroquímica.
El hidrógeno producido mediante electrólisis es una alternativa sostenible para el almacenamiento de energía eléctrica en forma de gas combustible para su posterior utilización en pilas de combustible, motores de combustión interna o turbinas de gas. No obstante, desde la perspectiva del ahorro de energía, toda transformación energética conlleva pérdidas.
El proceso de electrólisis es similar al proceso de carga de una batería.
El material del ánodo suele ser níquel o cobre recubierto con óxidos de manganeso, tungsteno, rutenio o platino. Estos metales favorecen la rápida combinación del oxígeno atómico para dar lugar a la formación de oxígeno molecular en su superficie. El cátodo es habitualmente de níquel, recubierto con cantidades menores de platino como catalizador para aumentar la velocidad de producción de hidrógeno. Se utiliza un separador de gas o diafragma, que permite el paso de iones, para evitar que el hidrógeno y oxígeno formados se mezclen y vuelvan a reaccionar.
La cantidad de hidrógeno que se produce en los electrolizadores está directamente relacionada con la densidad de corriente eléctrica que es capaz de gestionar, se define como la cantidad de corriente dividida por el área de electrodo. En general, cuanto mayor sea la densidad de corriente, mayor será la densidad necesaria para los electrodos, o en su defecto la tensión de alimentación requerida será mayor pero en este caso el coste energético por unidad de masa de hidrógeno producido aumentará.
Los electrolizadores en forma de Stack no son fiables sometidos a presión, cambios bruscos de la densidad de corriente. Los Stacks tienen rendimientos energéticos de menos del 65% y sin contar el 15% de gasto energético adicional por la necesidad de incorporar equipos auxiliares.
RENDIMIENTO DE UN ELECTROLIZADOR
Para comparar y evaluar el rendimiento de un sistema de electrólisis de agua se considera la producción de hidrógeno frente a la energía eléctrica total (total quiere decir TOTAL, de toda la planta contando con los dispositivos auxiliares) aplicada al sistema, tanto en términos de producción de hidrógeno como de energía contenida en términos del producto del hidrógeno producido por su poder calorífico inferior (si no se recupera el oxígeno) y superior (si se logra almacenar el oxígeno en relación estequiométrica).
Los actuales electrolizadores de celdas apiladas (Stacks) operan mal en un amplio rango de potencias o con cargas parciales, no son aptos para aprovechar los excedentes variables de electricidad.
Las celdas electrolíticas se suelen agrupar en serie formando apilamientos con el fin de elevar la tensión de trabajo formando una pila electrolítica, son grandes y pesadas para ser manejadas y su estructura de diseño implica la incapacidad de manejar altas presiones y temperaturas.
El rendimiento de los electrolizadores está determinado por la cantidad de energía que se requiere suministrar por cada unidad de volumen de hidrógeno producido. Las unidades que se suelen utilizar son los kWh/Nm3 o kWh/kg de hidrógeno. El máximo rendimiento que podrá alcanzar un electrolizador será entonces el correspondiente al contenido energético del hidrógeno almacenado en comparación, con toda la energía que se ha consumido en el proceso.
ELECTROLIZADORES MÁS FIABLES CON DIFERENCIA
Los electrolizadores alcalinos se han estado comercializando desde hace alrededor de un siglo y son los más extendidos. Sus celdas se componen de los dos electrodos, un separador microporoso denominado diafragma y un electrolito consistente en en una disolución acuosa de un 25–30 % de hidróxido de potasio (KOH) o de sodio (NaOH). Generalmente, se prefiere el hidróxido de potasio en comparación con el hidróxido de sodio (NaOH), ya que es más conductor pero a su vez es más corrosivo.
Los electrolizadores alcalinos comerciales operan a temperaturas comprendidas entre 80 y 150 ºC. La densidad de corriente típica es de 100–300 mA/cm2 y se alcanzan rendimientos de un 40–45 % sobre el hidrógeno obtenido a presión de trabajo. Las escasas presiones operativas de esta tecnología habitualmente están comprendidas entre 3 bar y 15 bar.
PERDIDAS POR COMPRESIÓN
El trabajo de compresión es variable y no sólo depende de la presión final, sino también del tipo de transformación y de la tecnología empleada. Una forma conveniente de valorar el coste de la energía necesaria para la compresión del hidrógeno es expresarla en forma de porcentaje sobre la energía total contenida en el hidrógeno almacenado. En la práctica, se utilizan compresores multietapa y los valores se sitúan en que para comprimir 1 kg de hidrógeno desde presión atmosférica hasta 200 y 700 bar con un compresor multietapa se requieren aproximadamente entre un 15 % y 18 % del hidrógeno almacenado después del proceso de electrólisis.
Estos datos son teóricos pues la a energía teórica se refiere al máximo permitido por la termodinámica (en un mundo perfecto donde todo sale bien), sin considerar pérdidas de transmisión ni rendimientos de conversión posteriores, por lo que, en la práctica, la compresión puede llegar a representar valores mucho mayores con respecto al contenido energético del hidrógeno almacenado, entre el 22% y el 38% debido a las perdidas por purga de silos de secado, que son necesarios para aumentar la pureza del hidrógeno antes de entrar a los compresores, estos a su vez consumen mucha energía para funcionar por la baja densidad del hidrógeno.
RECIPIENTE DE ALMACENAMIENTO
El Hidrógeno se almacena en depósitos cilíndricos similares a los utilizados para el almacenamiento de gas natural comprimido.
La exposición constante al hidrógeno provoca un fenómeno conocido como fragilización por hidrógeno en muchos materiales. El hidrógeno es un elemento muy reactivo, con gran tendencia a combinarse con las sustancias metálicas, provocando cambios en su red cristalina y en sus propiedades mecánicas, como pérdida de resistencia y ductilidad, que pueden ocasionar la iniciación o propagación de fracturas metálicas.
El almacenamiento de hidrógeno a presión requiere materiales especiales que sean resistentes al ataque corrosivo por hidrógeno, que tiene principalmente dos formas. Una de ellas se denomina carburación superficial y ocasiona una pérdida de resistencia. La otra forma de corrosión es la descarburación interna, que ataca desde el interior del acero, provocando una pérdida de ductilidad. Los ciclos de carga y descarga producen desgaste por estrés y debilitan el almacenamiento
HIDRÓGENO EN FORMA DE AMONÍACO
Un vector energético que puede ser la revolución del hidrógeno es el amoníaco (NH3).
El amoníaco producido a partir de hidrógeno verde se puede considerar amoníaco verde y su combustión no genera CO2. Si bien la combustión de amoníaco tiene algunos otros inconvenientes como la posible generación de óxidos de nitrógeno, hay técnicas para reducirla, y las ventajas frente al hidrógeno puro son múltiples. Por un lado, su transporte y almacenamiento requieren condiciones menos extremas, y por otro, se puede utilizar para generar electricidad con celdas de combustible similares a las del hidrógeno o quemar en una turbina como el gas.
El proceso de Haber es la reacción de nitrógeno e hidrógeno gaseosos para producir amoníaco. La importancia de la reacción radica en la dificultad de producir amoníaco a un nivel industrial.
El proceso Haber debe seguir una serie de pasos muy controlados y que requieren de mucho cuidado, el hidrógeno y el nitrógeno se bombean, a un compresor, a través de tuberías. La mezcla de hidrógeno y nitrógeno a una presión de 200 atm se eleva a una temperatura de 450°C. Los gases se bombean a un reactor que contiene un catalizador de hierro y se enfrían en el tanque de enfriamiento, el nitrógeno y el hidrógeno que no han reaccionado se reciclan y vuelven al reactor para que no se desperdicien y el amoníaco se licua y se separa.
Cuando el amoníaco se produce por la reacción entre el hidrógeno y el nitrógeno, se dice que la reacción es reversible. Esto significa que el amoniaco puede volver a convertirse en nitrógeno e hidrógeno.
Más allá del uso del amoníaco verde como vector energético, hay que tener una visión más amplia sobre el mismo y pensar que, compuestos como el propio amoníaco son ampliamente utilizados en la industria química y de fertilizantes. Este sistema de almacenamiento estable se ha de tener muy en cuenta.